 |
国家兽药产业技术创新联盟 National veterinary drug industry technology innovation alliance |
用户登录
联系我们
|
服务创造价值、存在造就未来
近日,中国农业科学院兰州兽医研究所口蹄疫与新发病流行病学团队解析了非洲猪瘟病毒(ASFV)在猪体内感染的靶细胞,以及在靶细胞内延长感染(Prolonged infection)的机制。
相关研究结果以“Single-cell profiling of African swine fever virus disease in pig spleen reveals viral and host dynamics”为题,发表于《美国科学院院报》(PNAS)。
非洲猪瘟是危害世界养猪业的“头号杀手”,然而,ASFV在猪体内真实生理环境下感染的靶细胞以及其在靶细胞内延长感染的机制仍不明确。
针对此问题,该研究利用单细胞测序,结合流式细胞术、多色组织芯片和体外感染鉴定等多种技术,对ASFV 感染过程中脾脏细胞类型组成的动态变化、感染细胞嗜性,调控免疫应答和抗病毒反应规律,以及其延长感染机制等方面进行了研究。
该研究首先建立了ASFV对猪感染致死的模型,测定了各组织感染指标的消长规律,表明脾脏是病毒载量最高的器官,因而选择病毒感染猪的脾脏进行单细胞测序。
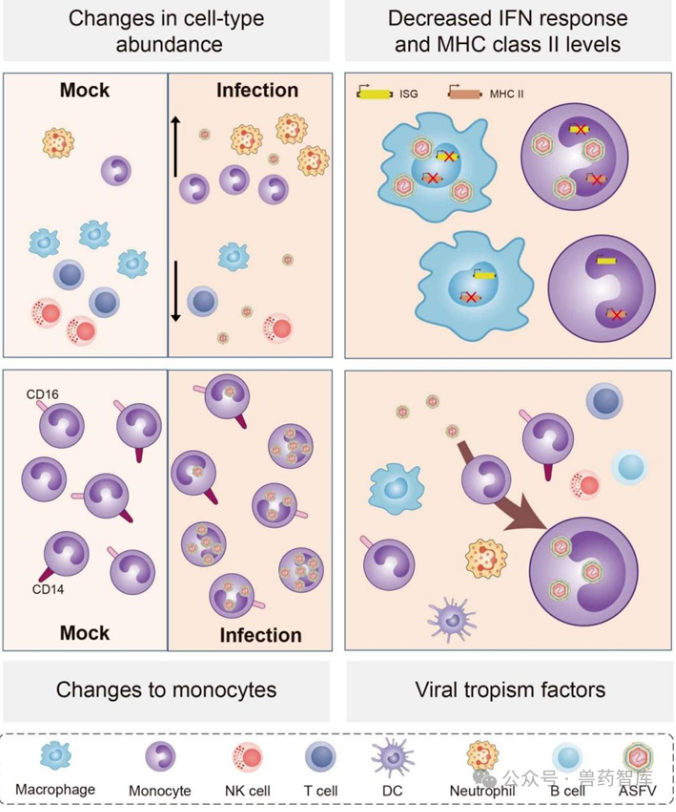
进一步深入分析及实验验证,确定了巨噬细胞和单核细胞是脾脏中感染ASFV的主要细胞类型。ASFV感染造成巨噬细胞大量死亡,一种罕见的单核细胞亚群成为了病毒感染的主要群体,对该群单核细胞进行谱系分析表明,它们是由骨髓紧急运输而来的未成熟单核细胞,该群细胞均未表达或低表达单核细胞的标记分子CD14。
对该靶细胞分析发现,细胞凋亡、干扰素反应和抗原呈递能力在这些单核细胞中被显著抑制,这有利于ASFV在猪体内的感染延长。
由于该群未成熟的细胞不表达经典的单核细胞标志分子CD14,因此,到目前为止,未成熟单核细胞作为ASFV重要靶细胞的还未被发现,也没有报道。
另外,ASFV感染细胞及旁观者细胞中MHC II类基因在整个ASFV感染过程中均显著下调表达,进而为揭示ASFV抑制抗原递呈的机制和中和抗体无法产生的原因提供了重要基础。
该研究系统阐明了ASFV感染的细胞嗜性、病毒复制和感染动态,以及激发免疫反应的特征,为ASFV感染路径的鉴定和感染致病机制的阐明提供了重要数据。
来源:兰兽研,中国农业科学院兰州兽医研究所郑海学研究员为本文通讯作者,朱紫祥研究员、毛箬青博士和刘保红博士为本文共同第一作者。该研究得到国家重点研发计划、国家自然科学基金、国家生猪产业体系、中国农业科学院科学中心重大任务、甘肃省科技重大专项等项目资助。大畜牧。
国家兽药产业技术创新联盟 National veterinary drug industry technology innovation alliance |
扫一扫  |
| 联系电话:010-62103991转611 联系地址:北京市海淀区中关村南大街8号 备案:京ICP备20024024号 |